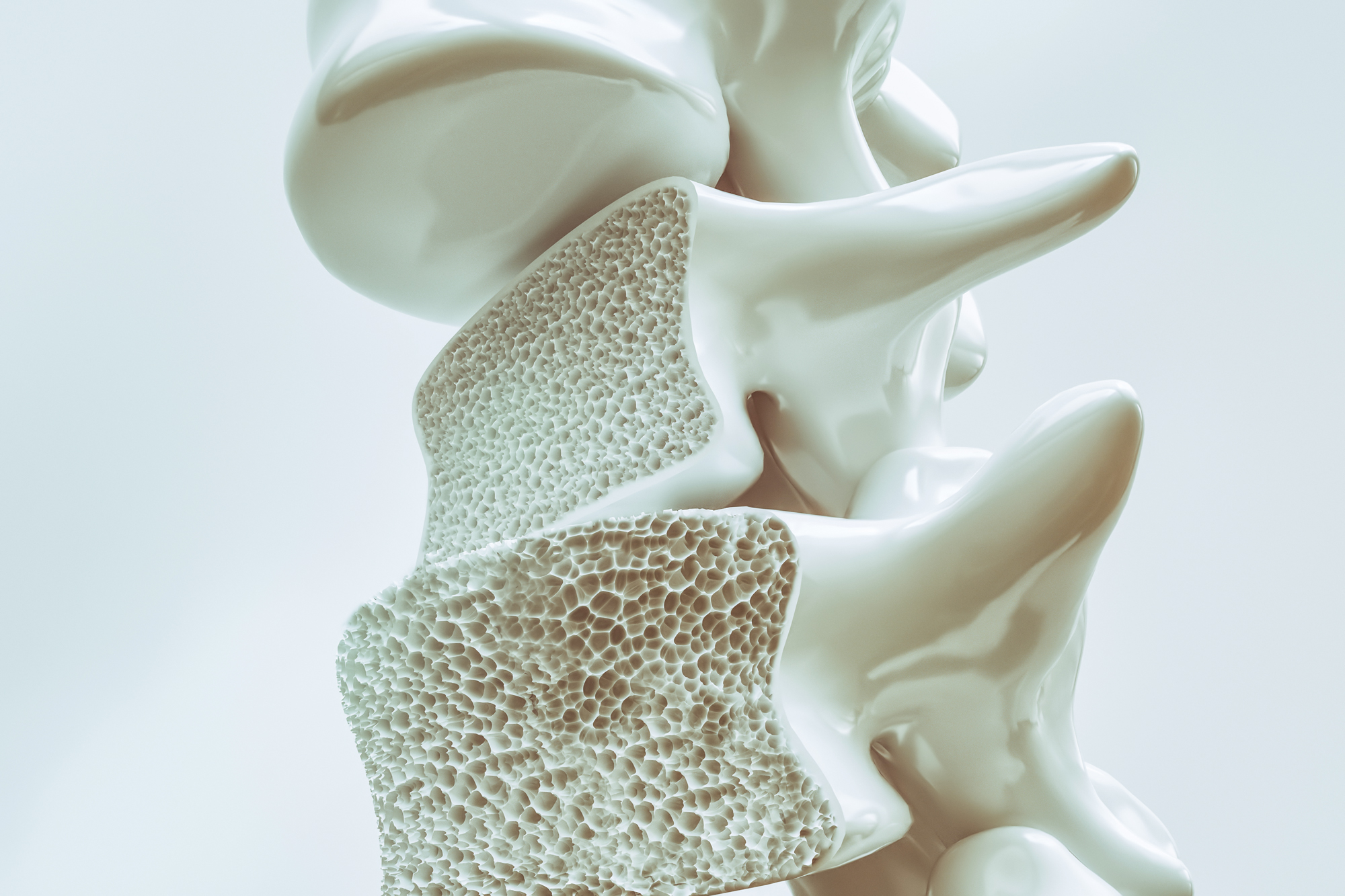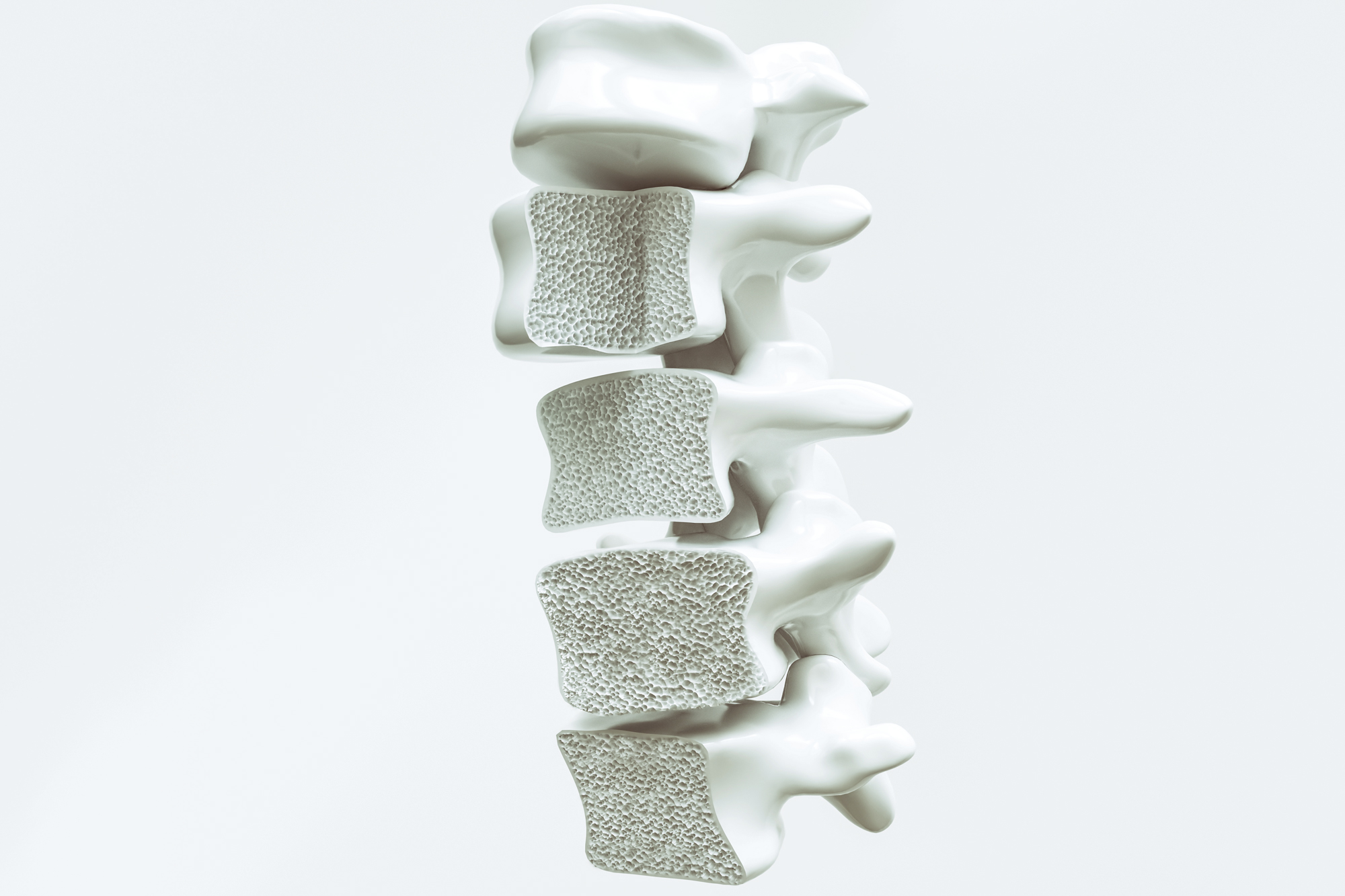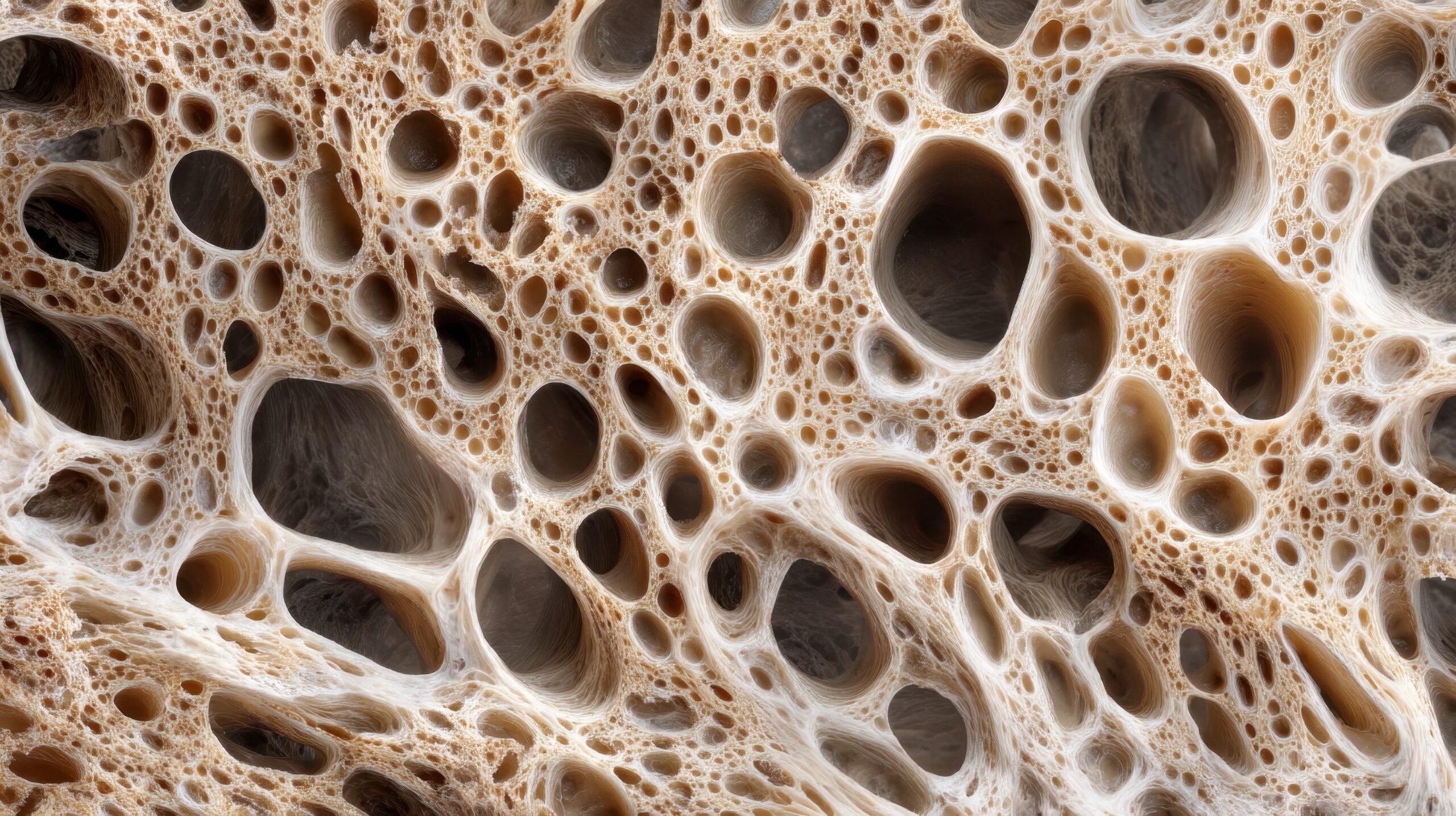
Der schleichende Verlust der Knochensubstanz
Etwa bis zum 30. Lebensjahr bauen wir Knochenmasse auf. Diese bleibt im Normalfall bis ca. zum 50. Lebensjahr konstant, danach nimmt sie auch beim gesunden Menschen ab. Ist der Abbau stärker als „normal” und auch die Feinstruktur des Knochens gestört, spricht man von Osteoporose. Osteoporose ist die häufigste Erkrankung des Knochenstoffwechsels und kann lange unbemerkt bleiben. Experten schätzen, dass in Österreich ca. 370.000 Frauen und 90.000 Männer betroffen sind.
Arten der Osteoporose
Osteoporose ist nicht gleich Osteoporose
Östrogene sind die Hormone mit dem größten Einfluss auf den Knochenstoffwechsel. Bei prämenopausalen Frauen ist das von den Ovarien produzierte 17ß-Estradiol (E2) das bedeutsamste, während in der Postmenopause das Östrion (E1) an Bedeutung gewinnt. E1 wird in zahlreichen Geweben gebildet, u.a. im Knochen.
Die Menopause einer Frau ist der Zeitpunkt, wo ihre Fortpflanzungsfähigkeit endet. Durch die Abnahme der ovariellen Geschlechtshormonproduktion kommt es zu einem klinischen Komplex, der kardiovaskuläre und urogenitale, aber auch osteologische Veränderungen nach sich zieht.
Während die natürliche Menopause der Frau im Schnitt zwischen dem 45. Und 55. Lebensjahr auftritt, steigt parallel dazu die Lebenserwartung weiter. Diese epidemiologische Entwicklung führt dazu, dass viele Frauen zumindest 3 Lebensdekaden ohne Einfluss der natürlichen Östrogene leben und altern. Dies ist nahezu gleichbedeutend mit einem Drittel der Gesamtlebenserwartung einer Frau.
Hochrechnungen zufolge sind in Deutschland über 6 Millionen Menschen von Osteoporose betroffen. Zwar sind dabei die über 5 Millionen Frauen die klare Mehrheit, aber mit über einer Million betroffenen Männern allein in Deutschland ist die männliche Osteoporose keine Nischenerkrankung.
Zur Früherkennung der Osteoporose müssen Patienten mit einem hohen Frakturrisiko identifiziert werden, um zukünftige Frakturen durch therapeutische Interventionen zu verhindern.
Ein flächendeckendes Screening ist nur durch die systematische Erfassung von Osteoporose-Risikofaktoren möglich, um Patienten zu selektieren, die einer weiteren Abklärung mittels Laboruntersuchungen und radiologischer Diagnostik inklusive Knochendichtemessung zugeführt werden sollten.
Das therapeutische Spektrum zur Behandlung der männlichen Osteoporose hat sich in den letzten Jahren günstigerweise erheblich erweitert und umfasst Therapeutika sowohl mit antiresorptiver als auch osteoanaboler Wirkung.
Bei der Abklärung der männlichen Osteoporose ist aufgrund des hohen Anteils „sekundärer Osteoporosen“ nach Risikofaktoren zu fahnden. Neben der üblichen Labordiagnostik sollte ein Sammelurin auf Kalzium durchgeführt werden, um eine idiopathische Hyperkalziurie zu erkennen. Durch die hohe Frakturprävalenz einerseits und die hohe Komorbidität hinsichtlich degenerativer Wirbelsäulenerkrankungen bei Männern ist eine Bildgebung der Wirbelsäule indiziert.
Die juvenile idiopathische Osteoporose (JIO) ist eine seltene, selbstlimitierende Erkrankung, die meist im Grundschulalter beginnt und ihren Abschluss mit Ende der Wachstumsphase findet. Die Diagnose wird durch den Ausschluss anderer Ursachen einer Skelettinstabilität gestellt und kann durch osteodensitometrische Verfahren untermauert werden. Die Behandlung ist an Patienten mit einer Osteogenesis imperfecta angelehnt und besteht bei schweren Formen aus einer intravenösen Bisphosphonatbehandlung.
Glukokortikoide haben einen sehr hohen Stellenwert bei der Behandlung verschiedener Erkrankungen. Aktuell wird etwa 1% der Bevölkerung in den entwickelten Ländern mit Glukokortikoiden behandelt. Ihre Hauptwirkungen bestehen in Entzündungshemmung und Immunsuppression/-modulation. Hier entfalten sie ausgeprägte und therapeutisch wichtige Wirkungen, die bei ihrer Einführung in die klinische Medizin vor mehr als 60 Jahren Anlass zur Euphorie gaben. Bald aber erkannte man, dass diese Medikamente auch unerwünschte Wirkungen auslösen, insbesondere, wenn sie in höheren Dosen über längere Zeit appliziert werden. Die glukokortikoidinduzierte Osteoporose ist eine der wichtigsten dieser unerwünschten Wirkungen.
Bei Patienten mit entzündlich-rheumatischen Erkrankungen manifestiert sich nicht selten eine sekundäre Osteoporose, da viele der im Entzündungsprozess gebildeten Faktoren auch in den Knochenstoffwechsel eingreifen. Die Knochendichte ist dann vermindert und die Mikroarchitektonik des trabekulären Knochens so verändert, dass das Frakturrisiko erhöht ist. Um diesen Veränderungen therapeutisch begegnen zu können, hat das Verständnis um die zugrunde liegenden immunologischen Prozesse in den vergangenen Jahren zunehmend an Bedeutung gewonnen. Eine enge Verzahnung von Immunsystem und Knochenstoffwechsel scheint hierbei der zentrale Aspekt zu sein. So fungieren proinflammatorische Zytokine gleichzeitig als Stimulatoren der Osteoklastengenese und sind damit auch essenzielle Mediatoren der Knochenresorption.
Als Folge einer Vielzahl chronischer Erkrankungen kann es zu einem Verlust an Knochenmasse kommen. Die Erkrankungen müssen nicht unmittelbar zu einer Osteoporose führen. Ein wichtiges Charakteristikum ist, dass der Knochenverlust schleichend vonstatten geht und u.U. erst erkannt wird, wenn es bereits zu einer Fraktur gekommen ist oder eine Knochendichtemessung durchgeführt wird.
Zumeist tragen viele Faktoren zur Ätiologie der Knochenentwicklungsstörung bei chronischen Erkrankungen bei. Zu ihnen zählen die Inflammation, die Gabe von Medikamenten, die mangelnde körperliche Aktivität, Fehlernährung und Endokrinopathien.
Schilddrüsenfunktionsstörung als Ursache
Bei der Abklärung sekundärer Osteoporosen findet sich in 5,6 – 6,4% der Fälle eine Schilddrüsenfunktionsstörung. Eine Schilddrüsenfunktionsstörung ist ein Risikofaktor für eine erniedrigte Knochendichte und für osteoporotische Frakturen, unabhängig von Alter und Geschlecht.
In den letzten Jahren wurde die Bedeutung der diabetischen Osteopathie als Ursache von Fragilitätsfrakturen erkannt. Ein gemeinsames Merkmal der Knochenpathophysiologie bei Typ-1- und Typ-2-Diabetes ist eine verminderte Knochenneubildung. Allerdings ist die Knochendichte beim Typ-2-Diabetes – im Gegensatz zum Typ-1-Diabetes – oft erhöht; die Osteopathie bei Patienten mit Typ-2-Diabetes ist somit ein Paradigma für eine Beeinträchtigung der Knochenfestigkeit trotz hoher Knochendichte. Mit hochauflösenden bildgebenden Techniken wurde eine erhöhte kortikale Porosität als eine wichtige Ursache der verminderten Knochenfestigkeit identifiziert.
Die Querschnittslähmung verursacht insbesondere bei einem kompletten Ausfall der motorischen Funktionen einen plötzlichen und extremen Verlust der durch die Muskulatur auf den Knochen übertragenen mechanischen Kräfte. Aufgrund der fehlenden Verformungen des Knochens erfolgt entsprechend der Mechanostat-Therapie ein sofort einsetzender und extremer Knochenabbau, der zu einer Osteoporose sowie einem erhöhten Risiko von Frakturen ohne adäquates Trauma führt. Neben der fehlenden Muskelaktivität werden auch weitere Faktoren wie zum Beispiel eine Atrophie des vaskulären Systems und eine Gewebeazidose für die Verminderung der Knochendichte diskutiert. Eine pharmakologische Therapie z.B. mit Bisphosphonaten kann bei aktuell noch sehr eingeschränkter und widersprüchlicher Datenlage nicht allgemein empfohlen werden. Die Anwendung mechanischer Kräfte durch Stehen/Gehen mit Hilfsmitteln oder funktioneller Elektrostimulation (FES) kann zu einer Verlangsamung und Verminderung des Knochenabbaus führen.
Prophylaxe
Eine ausreichende Versorgung mit Kalzium und Vitamin D sowie gezielte hormonelle Maßnahmen können helfen, den Knochenabbau frühzeitig zu bremsen und das Risiko osteoporotischer Frakturen zu senken.
Zur Therapie eingesetzt wird Cholecalciferol (Vitamin D3); 1 μg Vitamin D3 entspricht 40 IE Vitamin D3. Die Einnahme soll mit den Mahlzeiten erfolgen, da dies die Resorption verbessert. Die Tagesdosis (z.B. 800 IE) kann auch als Wochenäquivalent gegeben werden (5.600 IE einmal wöchentlich). Im Einzelfall kann bei Malabsorption eine parenterale (intramuskuläre) Gabe von 100.000 IE Cholecalciferol notwendig sein. In einigen Mitgliedstaaten der Europäischen Union (z.B. Deutschland) ist ein derartiges Präparat zugelassen. Die Gabe der aktiven Form von Vitamin D – Calcitriol (1,25-Dihydroxycholecalciferol) – ist nur bei schwerer Niereninsuffizienz indiziert.
kann die MHT zur Prävention von vertebralen, nichtvertebralen und proximalen Femurfrakturen in Betracht gezogen werden. Vor Beginn einer MHT sind alle individuellen Risikofaktoren, inklusive kardiovaskuläres und thromboembolisches Risiko, zu berücksichtigen, insbesondere bei Frauen über 60, die ein erhöhtes Basisrisiko für ernste Nebenwirkungen haben. Nach Ende einer MHT ist eine neuerliche Risikobewertung sinnvoll.


Nicht-medikamentöse Prophylaxe
Sturz- und Sturzfolgen zu vermeiden und durch regelmäßiges Training mit Gewichts- und Widerstandsbelastung die Knochenfestigkeit zu erhalten, hilft Ihrer Knochenstruktur und dem Frakturrisiko gleichermaßen.
Knochenmineraldichteverlust in der Lendenwirbelsäule und im proximalen Femur.
- Progressives Widerstandstraining allein oder in Kombination mit Joggen, zügigem Gehen oder Aerobic verringern den Knochenmineraldichteverlust im proximalen Femur.
- Progressives Widerstandstraining in Kombination mit zügigem Gehen oder Tai Chi reduziert den Knochenmineraldichteverlust in der Lendenwirbelsäule.
- Kombinierte Übungsprogramme mit den Trainingszielen Flexibilität (= funktionelles Bewegungsausmaß der Muskeln und Gelenke), Körperbalance und Muskelkraft senken das Sturzrisiko und das damit zusammenhängende Frakturrisiko.
Spezifische Osteoporose Therapie
Wenn die Erkrankung bereits gesichert ist, stehen Medikamente zur Verfügung, die gezielt zur Reduktion des Frakturrisikos eingesetzt werden.
(SERM) der die Knochenresorption hemmt und das Frakturrisiko für vertebrale Frakturen reduziert (nicht für nichtvertebrale Frakturen und proximale Femurfrakturen; Raloxifen ist zugelassen für die Prävention und Therapie der Osteoporose bei postmenopausalen Frauen.
Ein bedeutender zusätzlicher Effekt ist die Reduktion des relativen Risikos eines invasiven (Östrogenrezeptor-positiven) ammakarzinoms15 um 79 %.
Eine unerwünschte Nebenwirkung ist die Erhöhung es thromboembolischen Risikos.
Bisphosphonate sind potente Inhibitoren der Knochenresorption. ie werden an metabolisch aktiven Umbaueinheiten m Knochen abgelagert und bewirken eine
Apoptose von Osteoklasten.
Die Resorptionsaktivität wird im Gesamtskelett deutlich gedämpft und das Frakturrisiko reduziert. Bei Bisphosphonaten wurde diese fraktursenkende Wirkung über einen Zeitraum von zumindest 3 bis 5 Jahren nachgewiesen. Die genaue Dauer der Behandlung ist unklar.
wird. Bei der Behandlung der postmenopausalen Osteoporose ist eine Reduktion von vertebralen und nichtvertebralen Frakturen inklusive proximaler Femurfrakturen über 3 bis 5 Jahre nachgewiesen . Die Behandlungsdauer ist unklar. Nach Absetzen von Denosumab scheint es im Gegensatz zu den Bisphosphonaten zu einem raschen Anstieg des Knochenumbaus und in weiterer Folge zu einer Abnahme der Knochenmineraldichte zu kommen. Kiefernekrosen sind bei dieser für Osteoporose zugelassene Therapie eine sehr seltene Nebenwirkung.
Beschleunigung der Reifung und Stimulierung von Osteoblasten. Anschluss an die anabole Reaktion des Knochens kommt es nach Beendigung der Teriparatid-Therapie wiederum zu einem gesteigerten Knochenabbau, weshalb eine sofortige Anschlussbehandlung mit einem Antiresorptivum unbedingt notwendig ist.